| Γλώσσα : |
|
| Εγκυκλοπαίδεια της κοινότητας |Εγκυκλοπαίδεια Απαντήσεις |Υποβολή ερωτήματος |Λεξιλόγιο Γνώση |Ανεβάστε τη γνώση |
Marine Φυσικοχημείας |
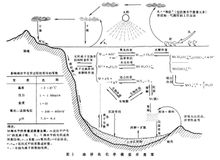        |
|
Ορισμούς Τεχνολογία Κινεζικό όνομα: Marine Φυσικοχημεία Όνομα: θαλάσσιο φυσικοχημείας Ορισμός: η χρήση των φυσικών και χημικών θεωρίες και τις μεθόδους της χημείας των ωκεανών και βιοχημικές επιστήμες προβλήματα.Εφαρμοσμένη επιστήμη: Θαλάσσιας Επιστήμης και Τεχνολογίας (ένα θέμα)? Marine Science (δύο άτομα)? Ωκεανό χημεία (δύο άτομα) Το ανωτέρω περιεχόμενο από το Εθνικό Επιστήμης και Τεχνολογίας Επιτροπή Έγκρισης ανακοίνωσε Ocean Marine Χημεία Φυσικοχημεία είναι ο πυρήνας της θεωρίας, εφαρμόζει τη θεωρία της φυσικής χημείας, άποψη και η μέθοδος για τη μελέτη των ωκεανών χημείας και γεωχημικών διεργασιών, συμπεριλαμβανομένου του νερού, τα αιωρούμενα σωματίδια και ιζήματα, τα επιφανειακά ύδατα και ιζήματα μικρο-πόρων νερού Η σύνθεση των άλλων θαλάσσιων συστημάτων, φυσικές και χημικές ιδιότητες και τη δομή του ωκεανού και του περιβάλλοντός του (ατμόσφαιρα, πυθμένα του ωκεανού, εκβολές ποταμών, κλπ.), το σύστημα που αποτελείται από φυσικές και χημικές διεργασίες που συμβαίνουν. Σύντομη Ιστορία της έρευνας 1959, που πραγματοποιήθηκε στη Νέα Υόρκη το συνέδριο διεθνείς θαλάσσιες μεταφορές, Theron είχε τον τίτλο " Θαλασσινό νερό φυσική χημεία "ομιλία αργότερα," θαλασσινό νερό φυσική χημεία, "το όνομα έχει υιοθετηθεί ευρέως. Ocean έγκαιρη ανάπτυξη της φυσικής χημείας, η μελέτη είναι κυρίως νερό, στη συνέχεια σταδιακά να επεκταθεί το πεδίο εφαρμογής της μελέτης των θαλασσίων ιζημάτων και άλλων διεπαφή , εξελίχθηκε σε ένα θαλάσσιο χημείας φυσικής. Marine Φυσικοχημείας, πρωτοποριακό έργο έχει πραγματοποιηθεί στις αρχές του 1900. 1901-1908, Knudsen και Ekman καθιέρωσε μία κλασική εξίσωση της κατάστασης του θαλασσινού νερού, το θαλασσινό νερό πυκνότητα, τη θερμοκρασία, την αλατότητα και την πίεση που συνδέεται με μια μαθηματική έκφραση? Αρχές του 1960, Theron, Galle Ουαλία και άλλοι σε χημικές θεωρίας της ισορροπίας και άλλες φυσικές αρχές χημικών, αυστηρή, συστηματική και ποσοτική εφαρμόζεται στον ωκεανό, η παρουσία των στοιχείων του εντύπου στο θαλασσινό νερό, το θαλασσινό νερό μοντέλο χημείας ιδρύθηκε για τη θαλάσσια Φυσική Χημεία έθεσε τα θεμέλια για τη δημιουργία και την ανάπτυξη. Μετά από αυτό το χρονικό διάστημα, τα μοντέλα χημεία του νερού (συμπεριλαμβανομένων των ιχνοστοιχείων σε διαλυμένη μορφή) έρευνα σε θαλάσσια χημεία της προσοχής του κοινού σε ένα περιεχόμενο της έρευνας. Από τη δεκαετία του 1960, οι άνθρωποι και πάλι ηλεκτροχημεία, χημική κινητική, κολλοειδών και χημείας των επιφανειών, η κβαντική χημεία και στατιστική θεωρία και πειραματικών μεθόδων που εφαρμόζονται στον ωκεανό, δεν έχει μελετηθεί μόνο η θαλάσσια υδάτινη μάζα, αλλά περιλαμβάνει επίσης θαλάσσια αναστολές, SML, ωκεάνια ιζήματα. Έρευνα Θαλάσσιο βασικά φυσικά και χημικά περιεχόμενο περιλαμβάνει: νερό Συντελεστής δραστηριότητα? Θαλασσινού μοντέλο χημεία? Ιχνοστοιχεία στο θαλασσινό νερό σωματιδίων υγρού στο στερεό - θεωρία της στερεάς διανομής? Πίεσης και θερμοκρασίας για την χημική ισορροπία των ωκεανών? Θαλασσινό νερό pH και οξειδοαναγωγής Προϋποθέσεις? δυναμική των ωκεανών των χημικών διεργασιών? θαλάσσια στοιχεία και να μείνουν μικροσκοπικά θαλάσσια έρευνα χημεία. Αμοιβαία σχέση Νερό υπάρχει μεταξύ των συστατικών του συμπλόκου σχέσης, εάν το νερό που ορίζεται ως «άλας» και ύδωρ, δύο συστατικών, το πρωταρχικό μέλημα μετά τρεις σχέσεις: ① η αλληλεπίδραση μεταξύ των μορίων του νερού, που είναι υγρό νερό διαρθρωτικά προβλήματα. Υγρό θεωρίες θεωρία, όπως δεσμοί υδρογόνου γίνεται twisted μοντέλο (θεωρία συνεχές), υποθέτει ότι ο πάγος γίνεται νερό, ο δεσμός υδρογόνου γίνεται πιο επιρρεπή σε κάμψη, το στρίψιμο και παραλλαγές, αλλά δεν έχουν ακόμη ανοίξει, συστροφή γίνεται διαθέσιμο υδρογόνο κλασική στατιστικές μεθόδους επεξεργασία? μοντέλο ταιριάζει κλουβί, υποθέτει ότι το υγρό γίνεται μια αυτο-συναρμολόγηση κλωβού, δηλαδή, τα μόρια σχηματίζουν δεσμούς υδρογόνου με πολλές από τις πεντάγωνο δωδεκάεδρο δικτύου που αποτελείται από έναν κλωβό, ο κλωβός συσκευασίας κοιλότητα κρυμμένα τα μόρια του νερού, αλλά δεν κάνουν με συγκόλληση δομή κλωβού? αναβοσβήνει μοντέλο συστάδες, οι οποίες υγρό νερό ως σύνδεση υδρογόνου των μορίων του νερού "αναβοσβήνει συστάδες" σε ένα ελαφρώς "ελεύθερη" μείγμα κολύμπι νερό, αυτή η επαφή μοντέλο με τη συνάρτηση κατανομής μαζί, η διαθέσιμη στατιστική μέθοδος για τον υπολογισμό μηχανική θερμοδυναμικές ιδιότητες, μετά από επανειλημμένες βελτιώσεις, που υπολογίζεται ελεύθερη ενέργεια, εσωτερική ενέργεια, εντροπία και τη θερμοχωρητικότητα των τιμών, σύμφωνα με τις μετρούμενες τιμές. Υπάρχουν δύο θεωρίες πίσω από το υβριδικό μοντέλο θεωρία. ② Θαλασσινό νερό "άλας" ιοντική αλληλεπίδραση με το νερό, την ενυδάτωση του ιόντος. Το αποτέλεσμα θα είναι ιοντική αγωγιμότητα και συντελεστή θερμοκρασίας, θερμοδυναμικών και κινητικών ιδιοτήτων της φύσης, η παρουσία των στοιχείων με τη μορφή του θαλασσινού νερού και της σταθερότητας του επηρεάζονται σε ποικίλους βαθμούς. ③ Θαλασσινό νερό "αλάτι" αλληλεπιδράσεις ιοντική. Διαθέσιμο ενεργότητα νερού και νερού συντελεστή συντελεστή διαπερατότητας να εκφραστεί. Οι τρεις σχέσεις, το πιο σημαντικό είναι ο συντελεστής δραστικότητας ποσό χαρακτηριστικό. Νερό συντελεστής δραστικότητας Και το γενικό νερό ή φυσικό νερό (ποτάμι, λίμνη, συντριβάνι, νερό) σε σύγκριση με ένα σημαντικό χαρακτηριστικό του νερού που περιέχει ένα μεγάλο αριθμό των αλάτων, η οποία καθιστά το νερό χαμηλής αλατότητος και ένα αραιό διάλυμα ανάμεσα στο άπειρο φυσικές - χημικές ιδιότητες υπάρχει μια μεγάλη διαφορά. Για να εκφράσουν το βαθμό της διαφοράς μεταξύ των δύο, στο θαλασσινό νερό που χρησιμοποιείται στις φυσικές και χημικές συντελεστή δραστηριότητας (κυρίως για διαλυμένης ουσίας) και νερό συντελεστή διαπερατότητας (χρησιμοποιείται κυρίως σε διαλύτη). Υπολογισμό της μέσης συστατικά θαλασσινού νερού και ξεχωριστή δραστηριότητα των ιόντων συντελεστής συντελεστής δραστικότητας των θεωρητικών μοντέλων και τύπων, υπάρχουν πολλές διαφορετικές ιόντων ένωση θεωρία, ειδικό μοντέλο αλληλεπίδρασης, Skate Childs τύπο, το μοντέλο ενυδάτωση, στατικά μοντέλα (συμπεριλαμβανομένων Davis τύπου), σύμπλεγμα αναπόσπαστο θεωρία επέκτασης, Spitzer τύπου και ούτω καθεξής. Αν και η χρήση των ιοντοεπιλεκτικά ηλεκτρόδια μπορεί να ληφθεί με ένα μόνο συντελεστή δραστηριότητας ιόντων, αλλά ακριβείς μετρήσεις αξία της και θεωρητικούς υπολογισμούς, ειδικά για ένα τέτοιο σύστημα υψηλής αλατότητας του νερού, δεν επιλυθεί εντελώς. Στην πράξη, οι διαθέσιμες ειδικές φόρμουλες αλληλεπίδρασης, όπως η Carter Childs τύπους και Spitzer άλλοι συντελεστές δραστηριότητας υπολογισμού του θαλασσινού νερού. Εν ολίγοις, ο παραπάνω τύπος μπορεί να συνοψιστεί στο ακόλουθο τύπο: όπου Debye - Huckel όρος αναφέρεται στη Debye - Huckel θεωρία ο νόμος περιορίζει τις υπολογισμένες τιμές. Σε αυτές τις διάφορες θεωρίες, προκειμένου να επεκτείνει το σύμπλεγμα αναπόσπαστο θεωρία εξίσωση και Spitzer βέλτιστα αποτελέσματα με τη μετρούμενη τιμή της διαφοράς στο πειραματικό φάσμα σφαλμάτων. Spitzer τύπος υπολογίζει όχι μόνο τη συνεχή συνιστώσα του θαλασσινού νερού συντελεστής δραστικότητας ιόντων, και μετά από την έλευση του τύπου Spitzer λίγο αργότερα εφαρμόζεται θαλάσσιων στοιχείων ίχνος χημικός στο θαλασσινό νερό ιοντικό υπολογισμό συντελεστή δραστηριότητα, τα αποτελέσματα με μια ειδική αλληλεπίδραση με μοντέλο υπολογισμού πιο συνεπής. Το 1982, αυτός ο τύπος έχει εφαρμοστεί με επιτυχία στη Νεκρά Θάλασσα (ιοντική ισχύ (±) Feng 10) στην κύρια δραστηριότητα υπολογισμού συντελεστή ιόντων. Spitzer πρότεινε τύπο, καθιστώντας το έργο των υπολογιζόμενων ειδικών συντελεστών δραστηριότητα σε μεγάλο βαθμό επιλυθεί. Θαλασσινό νερό μοντέλο χημείας Εκπόνηση μελέτης για την ύπαρξη στοιχείων στην γεωχημεία στοιχείο θαλασσινό νερό μορφή θαλάσσιας έρευνας, αλλά και να επηρεάσει τη διακύμανση στο θαλασσινό νερό της μετανάστευσης στοιχείο είναι ένας σημαντικός παράγοντας, έτσι ώστε το θαλασσινό νερό των ωκεανών χημεία μοντέλο γεωχημεία στοιχείο ένα σημαντικό μέρος. Είναι Θαλασσινό νερό ανάλυση των ιχνοστοιχείων σε μηχανισμό εκχύλισης θαλασσινό νερό ιχνοστοιχείων σε αλληλεπίδραση με το θαλασσινό νερό αιωρούμενα σωματίδια, κ.λπ., είναι συχνά θεωρείται προαπαιτούμενο. 1962, Galle Ουαλία και ME Thompson για τη μελέτη των βασικών στοιχείων στο θαλασσινό νερό διαλυμένη μορφή ζεύγους ιόντων προτεινόμενο μοντέλο. Αργότερα εκείνη η χημεία θαλασσινού νερού γκάμα των μοντέλων των εφαρμογών έχει περιοριστεί στα πάγια στοιχεία, αλλά και να επεκταθούν στα ιχνοστοιχεία και οργανική ύλη, και πρότεινε σύνθετο μοντέλο, HSAB (σκληρό και μαλακό οξεοβασική) μοντέλο, παραμέτρων του μοντέλου δραστηριότητα συντελεστή και τα μοντέλα μικροδομής . Τα μοντέλα αυτά χημικά μπορούν γενικά να χωριστούν σε τρεις κατηγορίες: ① Ο συντελεστής δραστηριότητας και συντελεστή διαπερατότητας για να περιγράψει την αλληλεπίδραση μεταξύ των ιόντων (π.χ. Μ. Whitfield με την εξίσωση Pitzer), να συναχθεί ορισμένες ιδιότητες του θαλασσινού νερού και των συστατικών του. Ωστόσο, αυτές οι μέθοδοι δεν έχουν τα γενικά θαλάσσια φαρμακεία συνηθίσει να απεικονίσει τη δομή των σχημάτων. ② ζεύγους ιόντων του μοντέλου ή σύνθετο μοντέλο. Theron, Galle Ουαλίας και Thompson πρότεινε για πρώτη φορά. Στην γνωστή χημική σύνθεση του θαλασσινού νερού, πολύπλοκες σταθερές σταθερότητας και συντελεστές δραστηριότητας με βάση την εφαρμογή των υπολογισμών χημική θεωρία ισορροπίας, έχουμε σημαντικά στοιχεία και τα μοντέλα χημείας ιχνοστοιχεία. ③ μοντέλο παράμετρος μικροδομή καθορίζεται από Zhang Zheng-Bin, Liu Liansheng, Chen Zhendong πρότεινε. Χημεία των ιχνοστοιχείων στο θαλασσινό νερό από το μοντέλο και τη σχέση μεταξύ των δομικών παραμέτρων είναι ορατά μαλακή οξύ και ενδιάμεσο οξύ στοιχεία σχηματίζονται κυρίως Μ-Cl-τύπου συμπλοκών, είναι είναι μια σκληρά στοιχεία οξέος σχηματίζονται κυρίως Μ-ΟΗ-τύπου συμπλοκών. CA / EA τιμή 0,1 με τη μορφή των διαλυμένων στοιχείων για είναι πιο περίπλοκη, Μ-Cl,-ΟΗ Μ, Μ-CO3, Μ-SO4 μορφή σύμπλοκα ιόντα μπορεί να είναι παρόν. Στην περιοχή του στόματος, τα στοιχεία διαλυμένη μορφή κατ 'αρχήν, μπορεί επίσης να υπολογιστεί ως ανωτέρω, αλλά η συγκεκριμένη λειτουργία απαιτείται σημειωθεί εκβολές ποταμών σύσταση, το pH, η οξείδωση - condition μείωση, την ιοντική ισχύ, οργανική σύνθεση και το περιεχόμενο, να ανασταλεί το είδος ύλης και του περιεχομένου της και άλλους παράγοντες. Διαφορετικοί μελετητές έχουν προτείνει ένα σταθερό κλάσμα του νερού είναι περίπου δέκα είδη των μοντέλων χημικών, τα συμπεράσματα σε γενικές γραμμές παρόμοια, αλλά οι "M-Cl" ζεύγη ιόντων που δημιουργούνται σε αυτό το σημείο, υπάρχουν δύο αντίθετες απόψεις, τα περισσότερα μοντέλα δεν θεωρούν το "M- CL "ζεύγους ιόντων γενιάς, αλλά μερικά πειράματα και θεωρητικούς υπολογισμούς που μόνο θεωρούν" Μ-ΟΙ "ζεύγους ιόντων γενιάς, και ο ρυθμός παραγωγής της (%) μπορεί να είναι υψηλότερη από ό, τι το" M-SO42-ν "υψηλότερο. Αυτές οι δύο απόψεις δεν έχουν επανενωμένη. Η παρουσία ιχνοστοιχείων στο θαλασσινό νερό τυπικές πτυχές, υπάρχουν διαφορετικά συμπεράσματα μοντέλα διαφορετικές καταστάσεις. Για παράδειγμα, η βιβλιογραφία αναφερόμενη γενικά U (Ⅵ) στο θαλασσινό νερό διαλύονται σε μορφή UO2 (CO3) Rao 3, αλλά ορισμένοι Κινέζοι μελετητές μέσω πειραμάτων και θεωρητικών υπολογισμών αποδείχθηκε σημαντική παρουσία σε μορφή UO2 (ΟΗ) Yin, UO2 (CO3) Rao 3 φορές. Επιπλέον, η σημασία της αυξανόμενης σημασίας οργανικά συμπλέγματα, όπως ο χαλκός, ο ψευδάργυρος και άλλες υφιστάμενες μορφές της οργανικής από το 50% της συνολικής κατανομής, λαμβάνοντας υπόψη το σύνθετο σχηματισμό των οργανικών χημικών μοντέλο του νερού, έχει συμπεριληφθεί στην ημερήσια διάταξη της έρευνας. Στερεά νερό Σύντομη εισαγωγή Θαλασσινό νερό περιέχει μεγάλες ποσότητες στερεών σωματιδίων, με κολλοειδή χημεία ή χημικά χαρακτηριστικά επιφάνειας. Αυτά στερεό Ιχνοστοιχεία Σωματιδίων υγρών - στερεών διανομή, που ακολουθείται από χαμηλές συγκεντρώσεις της διεπιφανειακής χημείας και χημείας κολλοειδούς του νόμου. Αυτή η έρευνα είναι η διερεύνηση της μεταβολής του στοιχείου ωκεανών μετανάστευσης θεωρητική βάση είναι ένα σημαντικό χημικό περιεχόμενο των εκβολών ποταμών, αλλά και της θαλάσσιας ρύπανσης και της ρύπανσης, των πόρων θαλασσινό νερό εξόρυξη βασική χημεία της έρευνας. Παρά το γεγονός ότι οι περισσότερες έρευνες σε αυτό τον τομέα για τα ιχνοστοιχεία, αλλά και σημαντικά στοιχεία στο θαλασσινό νερό - η διεπαφή μεταξύ του ωκεανού δαπέδου ανταλλαγής ιόντων, ανήκουν επίσης στο πεδίο εφαρμογής αυτού του ρόλου, όπως ιζήματα ανθρακικού ασβεστίου - Mg ανταλλαγή Mg2 2 CaCO3 Gong Ca2 Μ.Ε.Π.Τ. (CO3) 2 Ένα άλλο παράδειγμα του pH θαλασσινού νερού μπορεί να έχει ένα σημαντικό ρόλο στο σχηματισμό των Κ -Η ανταλλαγής: |
| Χρήστης Ανασκόπηση |
|
Δεν υπάρχουν ακόμη σχόλια |